- Autor Alex Aldridge aldridge@what-difference.com.
- Public 2023-12-17 13:34.
- Naposledy změněno 2025-06-01 07:36.
Klíčový rozdíl mezi oxidem dusnatým a oxidem dusnatým je ten, že oxid dusnatý je bezbarvý plyn, zatímco oxid dusnatý je bílá pevná látka.
Oxid dusnatý a oxid dusnatý jsou chemické sloučeniny obsahující dusík a kyslík. Jedná se o oxidy dusíku. Mají však odlišné chemické a fyzikální vlastnosti.
Co je oxid dusnatý?
Oxid dusnatý je anorganická sloučenina s chemickým vzorcem NO. Říkáme tomu oxid dusnatý, protože je to oxid dusíku. Je to vlastně volný radikál, protože má nepárový elektron. Navíc je to heteronukleární dvouatomová molekula.
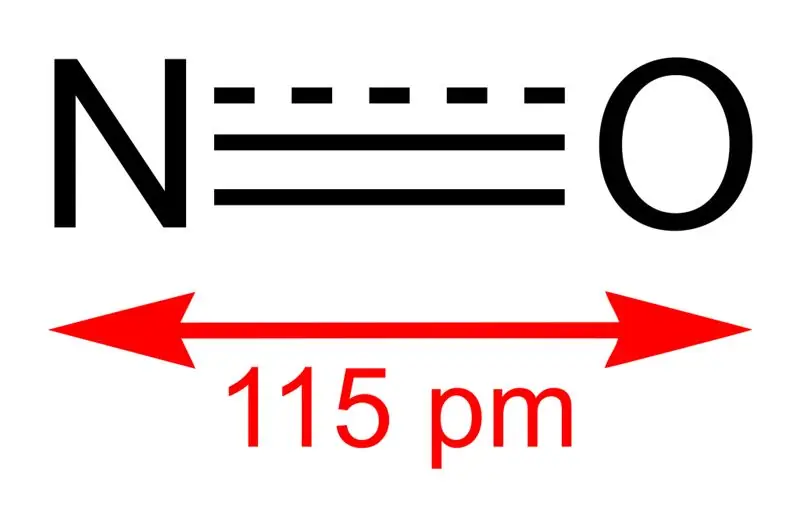
Obrázek 01: Struktura oxidu dusnatého a délka vazby mezi N a O
Molární hmotnost této sloučeniny je 30 g/mol. Vyskytuje se jako bezbarvý plyn. Navíc jeho bod tání je -164 °C, zatímco bod varu je -152 °C, což jsou velmi malé hodnoty ve srovnání s jinými oxidy dusíku. Tento volný radikál můžeme vyrobit oxidací amoniaku při 850 °C v přítomnosti platinového katalyzátoru. V laboratorním měřítku ji však můžeme připravit redukcí zředěné kyseliny dusičné mědí.
Co je oxid dusný?
Oxid dusný je anorganická sloučenina, která má chemický vzorec N2O5 Říkáme tomu oxid dusnatý. Je to binární oxid dusíku. Navíc je nestabilní a může působit jako nebezpečné oxidační činidlo. Molární hmotnost sloučeniny je 108,01 g/mol. Vyskytuje se jako bílá pevná látka.
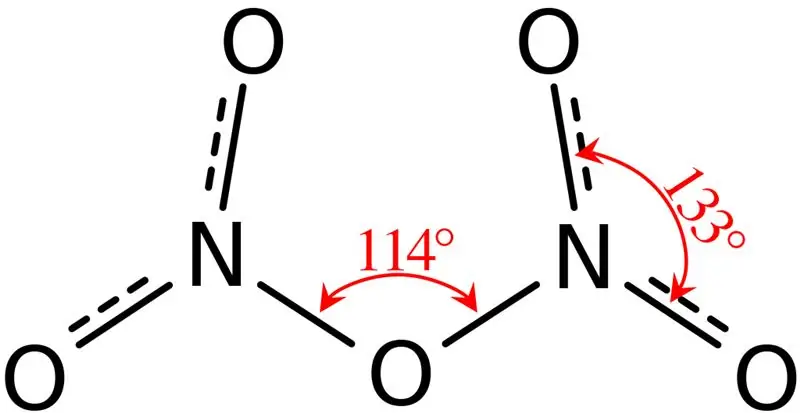
Obrázek 02: Struktura oxidu dusného
Navíc bod tání této sloučeniny je 41 °C a při 47 °C tato sloučenina podléhá sublimaci. Tato sloučenina reaguje s vodou za vzniku kyseliny dusičné. Molekulární tvar molekuly oxidu dusného je navíc rovinný. Tuto sloučeninu můžeme vyrobit dehydratací kyseliny dusičné s oxidem fosforečným.
Jaký je rozdíl mezi oxidem dusnatým a oxidem dusnatým?
Oxid dusnatý je anorganická sloučenina, která má chemický vzorec NO, zatímco oxid dusnatý je anorganická sloučenina, která má chemický vzorec N2O5 Klíčový rozdíl mezi oxidem dusnatým a oxidem dusnatým je v tom, že oxid dusnatý je bezbarvý plyn, zatímco oxid dusnatý je bílá pevná látka. Navíc můžeme oxid dusnatý vyrábět oxidací amoniaku při 850 °C v přítomnosti platinového katalyzátoru. Výroba oxidu dusného se však provádí dehydratací kyseliny dusičné oxidem fosforečným. Při zvažování tvaru molekuly je oxid dusnatý lineární, zatímco oxid dusnatý je rovinný.
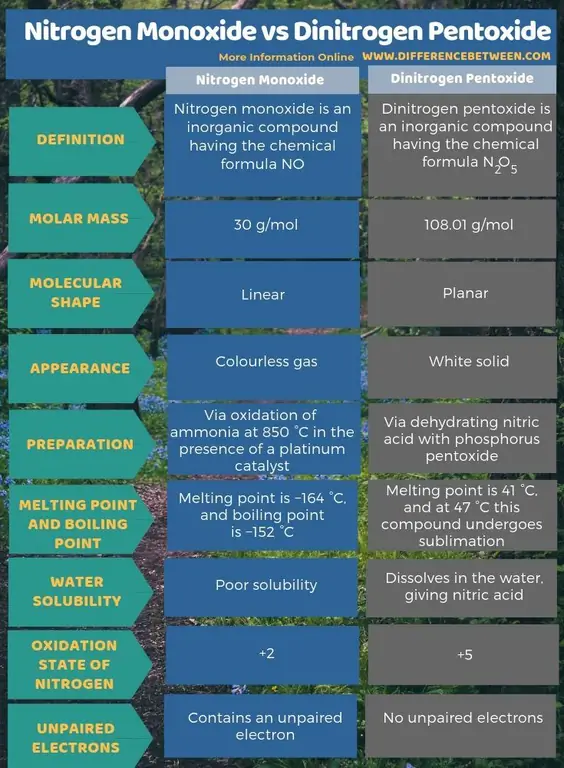
Shrnutí - oxid dusnatý vs oxid dusnatý
Oxid dusnatý je anorganická sloučenina, která má chemický vzorec NO, zatímco oxid dusnatý je anorganická sloučenina, která má chemický vzorec N2O5 Klíčový rozdíl mezi oxidem dusnatým a oxidem dusnatým je ten, že oxid dusnatý je bezbarvý plyn, zatímco oxid dusnatý je bílá pevná látka.






