- Autor Alex Aldridge aldridge@what-difference.com.
- Public 2023-12-17 13:34.
- Naposledy změněno 2025-06-01 07:36.
Klíčový rozdíl mezi kyselinou uhličitou a hydrogenuhličitanem je ten, že kyselina uhličitá je neutrální chemická sloučenina, zatímco hydrogenuhličitan je záporně nabitá chemická sloučenina.
Kyselina uhličitá je slabá kyselina, která se tvoří v roztoku, když se oxid uhličitý rozpustí ve vodě, s chemickým vzorcem H2CO3. Hydrogenuhličitan vzniká kombinací tří atomů kyslíku, atomu vodíku a atomu uhlíku s chemickým vzorcem HCO3-.
Co je kyselina uhličitá?
Kyselina uhličitá je H2CO3. Někdy dáváme tento název roztokům obsahujícím oxid uhličitý rozpuštěný ve vodě nebo sycené vodě. Sycená voda totiž obsahuje malé množství H2CO3. Kromě toho je kyselina uhličitá slabá kyselina a může tvořit dva typy solí jako uhličitany a hydrogenuhličitany. Molární hmotnost této sloučeniny je 62,024 g/mol.
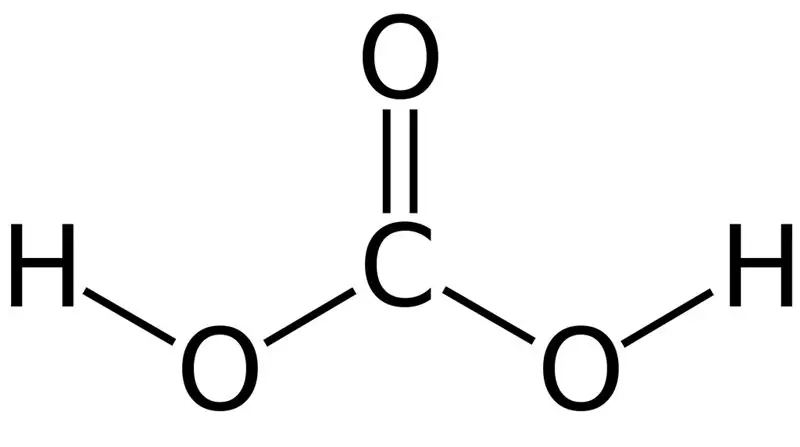
Obrázek 01: Chemická struktura kyseliny uhličité
Když se oxid uhličitý rozpustí ve vodě, vstoupí do rovnováhy mezi oxidem uhličitým a kyselinou uhličitou. Rovnováha je následující:
CO2 + H2O ⟷ H2CO3
Přidáme-li k zásadě přebytek kyseliny uhličité, získáme hydrogenuhličitan. Ale pokud je přebytek báze, pak má kyselina uhličitá tendenci vytvářet sycené soli. Přesněji řečeno, kyselina uhličitá je sloučenina karboxylové kyseliny, která má dva substituenty hydroxylové skupiny připojené ke karbonylovému uhlíku. Navíc je to polyprotická kyselina, která je schopna darovat protony. Má dva odnímatelné protony, takže je specificky diprotický.
Co je bikarbonát?
Bikarbonát vzniká kombinací tří atomů kyslíku, atomu vodíku a atomu uhlíku. Produktem této kombinace může být iont nebo sloučenina s více elektrony než protony. Můžeme jej popsat jako chemický druh mající chemický vzorec HCO3-.
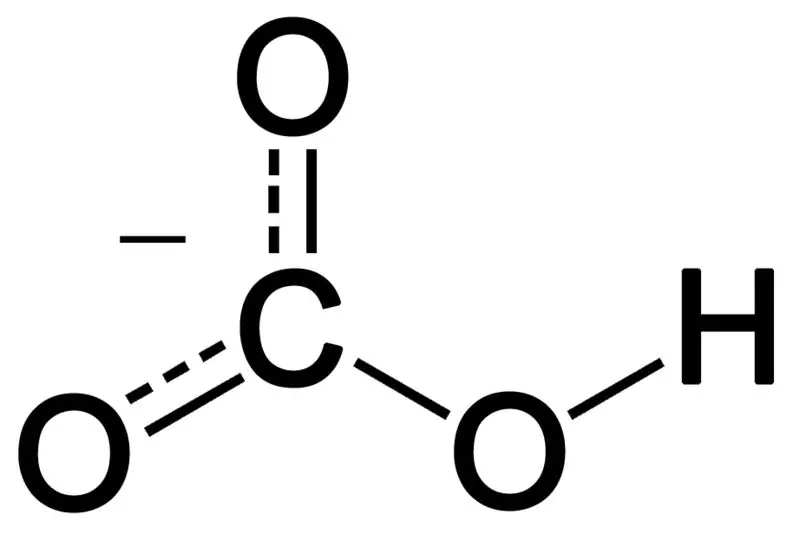
Obrázek 02: Chemická struktura bikarbonátového aniontu
Tato sloučenina je laicky řečeno klíčovou součástí pH pufrovacího systému těla: je zodpovědná za udržení krve ve stavu, který není příliš kyselý ani příliš zásaditý. Kromě toho slouží jako způsob, jak udržet trávicí šťávy pod kontrolou, jakmile žaludek dokončí trávení potravy. Kromě toho kyselina uhličitá v dešťové vodě vytváří hydrogenuhličitanové ionty, když narazí na skály. Tento tok hydrogenuhličitanových iontů je důležitý pro udržení uhlíkového cyklu v chodu.
Jaký je rozdíl mezi kyselinou uhličitou a hydrogenuhličitanem?
Kyselina uhličitá je slabá kyselina, která se tvoří v roztoku, když se oxid uhličitý rozpustí ve vodě, a její chemický vzorec je H2CO3. Hydrogenuhličitan vzniká kombinací tří atomů kyslíku, atomu vodíku a atomu uhlíku s chemickým vzorcem HCO3-. Klíčový rozdíl mezi kyselinou uhličitou a hydrogenuhličitanem je v tom, že kyselina uhličitá je neutrální chemická sloučenina, zatímco hydrogenuhličitan je záporně nabitá chemická sloučenina. Kromě toho se kyselina uhličitá používá při výrobě bublinkových, šumivých nápojů, při léčbě dermatitid, v ústní vodě atd., zatímco hydrogenuhličitan se používá v potravinových přípravcích, jako je pečení (jako kypřící činidlo), a dává schopnost odolávat změnám pH.
Následující infografika shrnuje rozdíl mezi kyselinou uhličitou a hydrogenuhličitanem ve formě tabulky pro srovnání vedle sebe.
Shrnutí - Kyselina uhličitá vs. Bikarbonát
Kyselina uhličitá je H2CO3. Hydrogenuhličitan vzniká kombinací tří atomů kyslíku, atomu vodíku a atomu uhlíku, s chemickým vzorcem HCO3-. Klíčový rozdíl mezi kyselinou uhličitou a hydrogenuhličitanem je v tom, že kyselina uhličitá je neutrální chemická sloučenina, zatímco hydrogenuhličitan je záporně nabitá chemická sloučenina.






